حل كتاب الكيمياء ثاني ثانوي ليبيا PDF
ملفات اخرى
-
اختبار
 امتحان نهائي رياضيات ثاني ثانوي الفصل الثاني ليبيا
امتحان نهائي رياضيات ثاني ثانوي الفصل الثاني ليبيا -
اختبار
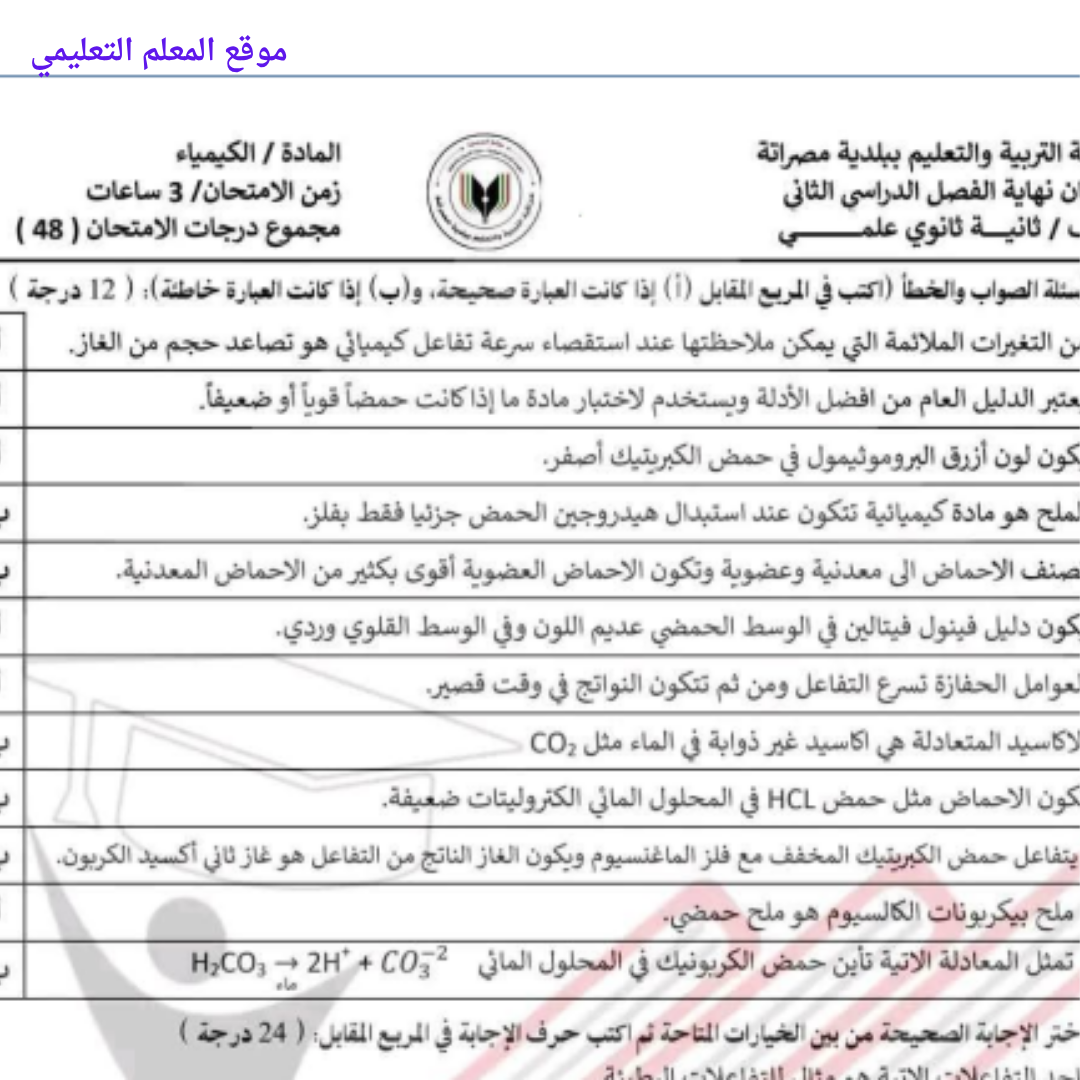 امتحان نهائي الكيمياء ثاني ثانوي الفصل الثاني ليبيا
امتحان نهائي الكيمياء ثاني ثانوي الفصل الثاني ليبيا -
اختبار
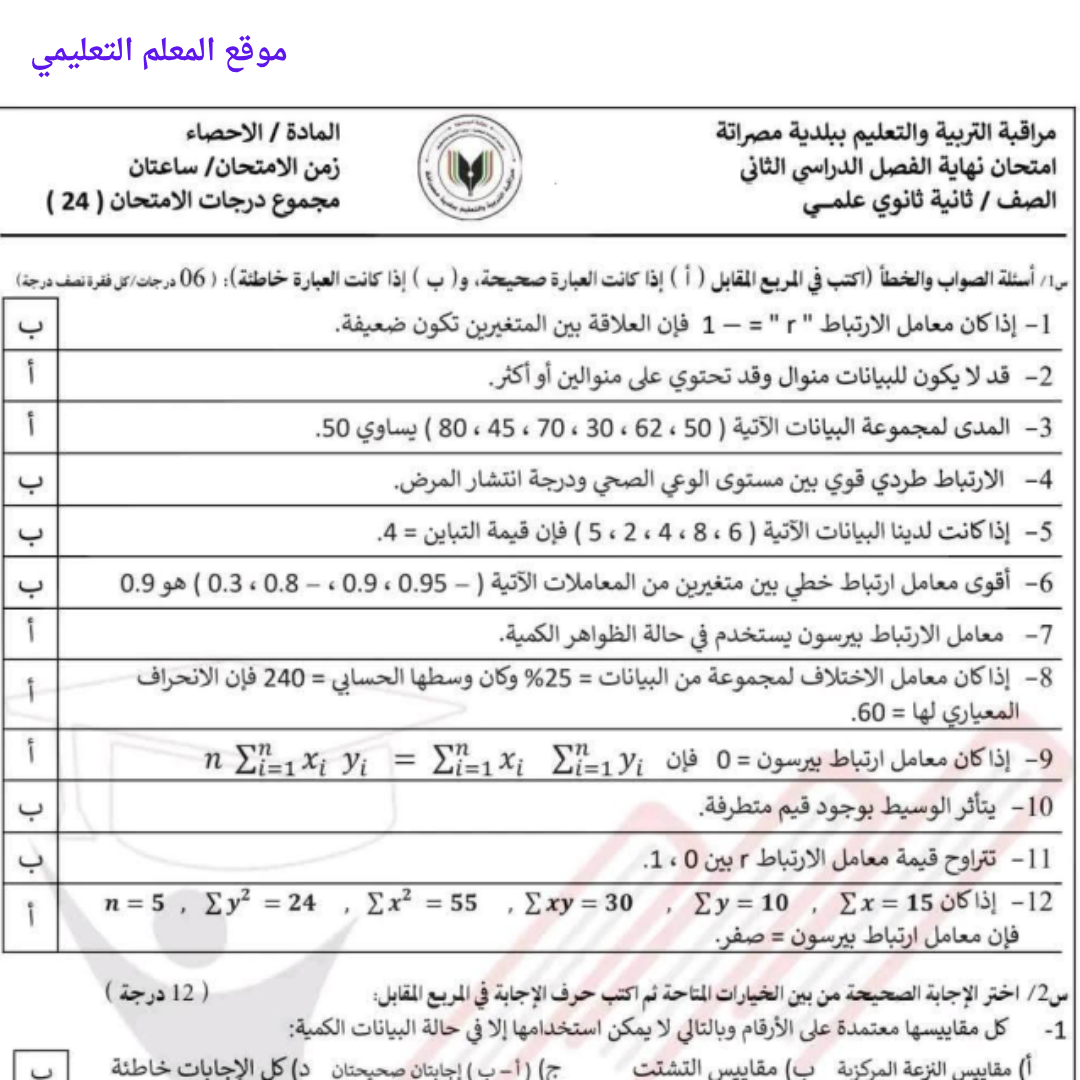 امتحان نهائي الاحصاء ثاني ثانوي الفصل الثاني ليبيا
امتحان نهائي الاحصاء ثاني ثانوي الفصل الثاني ليبيا -
اختبار
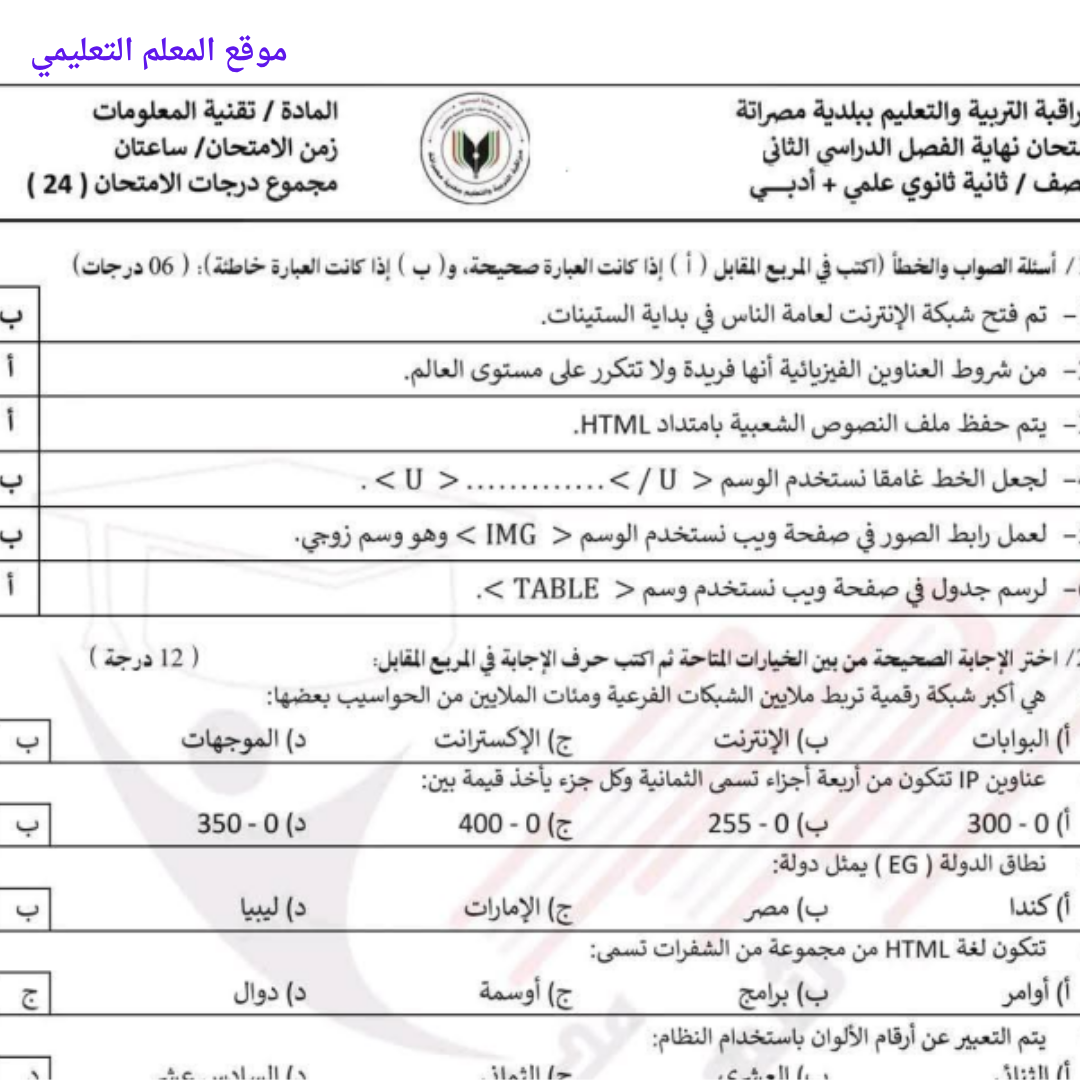 امتحان نهائي تقنية المعلومات ثاني ثانوي الفصل الثاني ليبيا
امتحان نهائي تقنية المعلومات ثاني ثانوي الفصل الثاني ليبيا -
اختبار
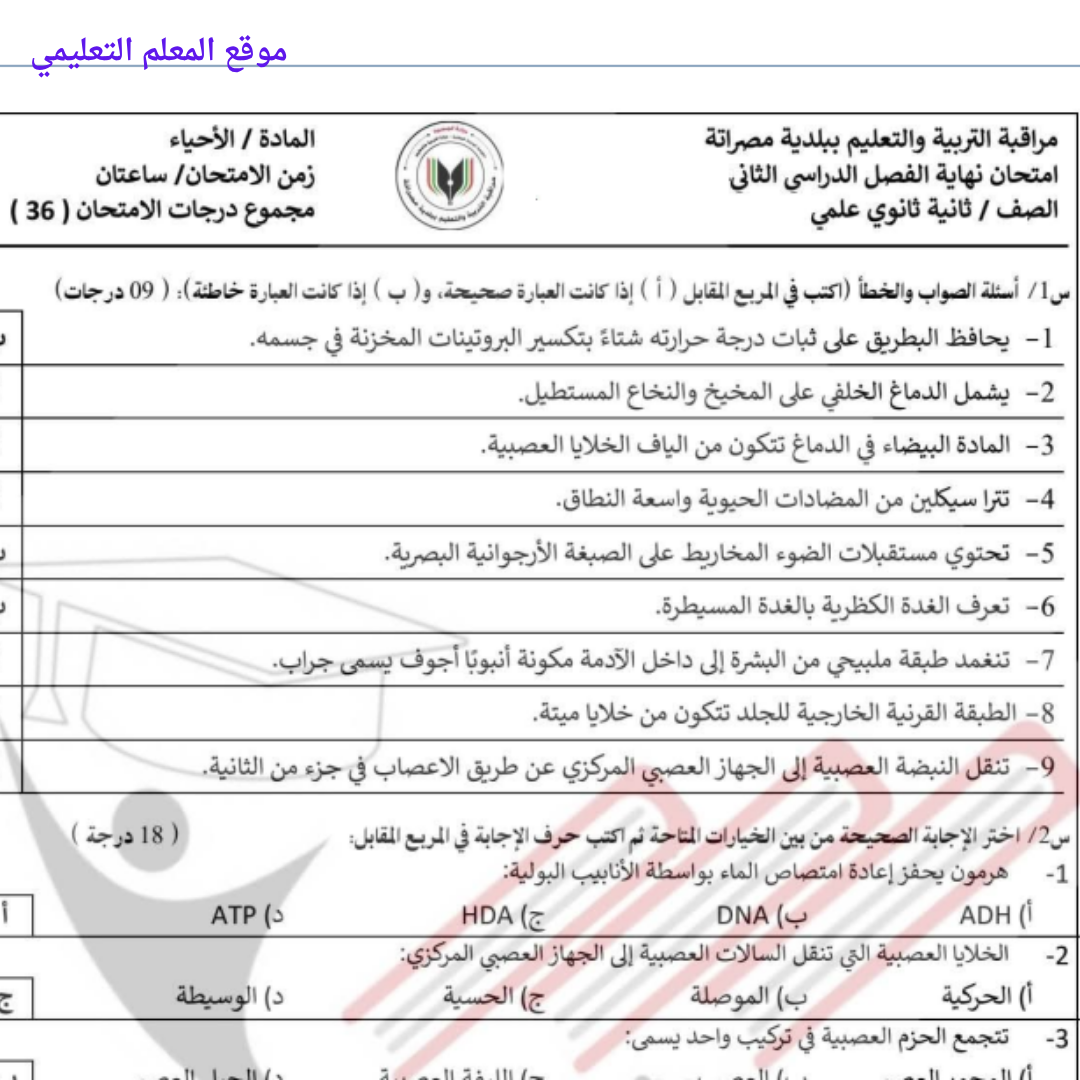 امتحان نهائي احياء ثاني ثانوي الفصل الثاني ليبيا
امتحان نهائي احياء ثاني ثانوي الفصل الثاني ليبيا -
اختبار
 امتحان نهائي التربية الاسلامية ثاني ثانوي الفصل الثاني ليبيا
امتحان نهائي التربية الاسلامية ثاني ثانوي الفصل الثاني ليبيا
هل تريد تنزيل حلول كتاب كراسة التدريبات كيمياء للصف الثاني الثانوي المنهج الليبي الجديد 1447- 2026 برابط تحميل مباشر ومجانا وبصيغة pdf.
حل كتاب كيمياء ثانية ثانوي ليبيا pdf, حل كتاب الكيمياء السنة الثانية منهج ليبيا الجديد pdf.
1- الأكسدة هي نزع لل الكترونات
2- العامل المؤكسد هو . للإلكترونات . المكتسب
3 الاختزال هو نقص في حالة . التأكسد
4 تفاعلات الاخسية يكون بها كل من الأكسدة والاختزال في نفس الوقت .
-5- يعتبر اكتساب الهيدروجين عملية. احتزال
ة العامل المختزل هو مانح للإلكترونات .
7- بر منجانات البوتاسيوم المحمضة هي عامل مؤكسد قوي .
خلال التحليل الكهربائي، تتضمن التفاعلات عند الـ كانون اختزالاً.
و خلال التحليل الكهربائي، تتضمن التفاعلات عند الـ . انود أكسدة.
10- يستخدم محلول يوديد البوتاسيوم كاختبار للعامل المؤكسد؛ لأنه يتحول من عديم اللون إلى اللون الأسود عند وجود العامل المؤكسد .
11- تستخدم ثانى كرومات بوتا البرتقالي إلى الأخضر في وجود هذه العوامل. بوتاسيوم : المحمضة كاختبار للعوامل المختزلة؛ لأنها تتحول من اللون
يتعلق السؤالان 12 و 13 بالتفاعل الكيميائي التالي :
. Cl₂ (g) + 2KBr (aq) → 2KCl (aq) + Br2 (1)
12- العامل المؤكسد هو الـ . الكلور
1- القطب المتصل بالطرف الـ للخلية يسمى الكاثود.
-2- الأيون الذي يتجه نحو الطرف الموجب للخلية، يعرف بالـ اكسدة
3 المواد الصلبة التي لا توصل الكهرباء تعرف بالـ الايون السالب
4- السوائل التي لا توصل الكهرباء تسمى سوائل .
العوازل غير الكتروليتية
5- الأحماض والقلويات المخففة التي تحتوي على أيونات قليلة هي . الكتروليت ضعيف
6- التحليل الكهربائي دليل على وجود الصلب وتكون حرة الحركة في حالة المصهور أو المحلول .
ايونات التي تتماسك في شكل شبكة في حالة
عند الانور غاز الاكسيجين
7- عند تحليل حمض الكبريتيك المخفف بين قطبين حاملين يكون الناتج
عبد الكاثود غاز الهيدروجين اكسده
8- إذا حللنا محلول كلوريد صوديوم مركز، فإن الناتج عند الكاثود هو غاز الهيدروجين
9- أثناء التنقية الكهربائية للنحاس، يعمل النحاس غير النفي كـ .انود
10- عند الطلاء الكهربائي للنحاس، يعمل الجسم المراد طلاءه كن
11 عملية اكتساب الإلكترونات عند الكاثود تعرف بالـ . الكاثودي.
12- العاملان الرئيسان اللذان يؤثران على نواتج التحليل الكهربائي هما ونوع الأقطاب المستخدمة.
إذا تم الحصول على التمثيل (ج) تحت شروط عادية، أي التمثيلات من (1 ) إلى ( و ) ينطبق عند :
1 - تبريد الحمض قبل إضافته للشرائح ؟
2 - تفاعل نصف كمية الشرائح فقط مع الحمض ؟ .
3 طحن شرائح الرحام إلى مسحوق ناعم قبل تفاعلها مع الحمض ؟
4- استخدام حمض هيدروكلوريك مركز ؟ .
5 - استخدام شرائح رخام لها حجم اكبر ( الضعف ) ؟
تدريب 5 - 4
تصف القطعة التالية كيفية استخدام الأحماض لتنظيف الفلزات التي فقدت بريقها. اقرأها وأجب عن الأسئلة التالية لها.
كثيرا ما تستخدم الأحماض كمنظفات في المنازل تتفاعل الأحماض مع القواعد، لذلك تستخدم لتنظيف الفلزات التي فقدت بريقها، وتصدأ الفلزات؛ لأنها تتفاعل مع الغازات الموجودة بالهواء وتتغطى بطبقة من الأكسيد أو الكبريتيد، ويوجد غطاء الأكسيد الشائع على أجسام الحديد والفولاد ويعرف بالصدا، ويسمى كيميائيا باكسيد الحديد (III) المائي ، Fe2OH). تحتوي عادة منظفات الصدأ على حمض معدني قوي كحمض الفوسفوريك (HPO) أو حمض الهيدروكلوريك (HCl). ولما كانت هذه الأحماض قوية، فإنها تكون خطرة ويجب استعمالها بعناية فائقة، يمكن نزع بقع الصدأ من على الملابس باستخدام حمض إيثان دايويك (COOH)، وهو حمض عضوي الاسم الشائع له حمض الأوكساليك ) أضعف من الأحماض المعدنية، مع ذلك أهم عيوبه كونه ساما. يمكن تنظيف فلزات أخرى باستخدام أحماض عضوية أقل سمية كحمض الأسيتيك (CH, COOH) أو حمض الستريك (CH). كلا هذين الحمضين يشيع استخدامهما في المنازل. الحل هو 65 محلول حمض الاسيتيك، ويوجد حمض الستريك في الفواكه الحمضية كالليمون والطريقة الفعالة لتنظيف جسم نحاسي هو حكه بقطعة ليمون، حيث تذوب طبقة الأكسيد وتكون سترات النحاس (II) التي يمكن غسلها بعد استخدام المنظفات الحمضية يكون من المهم غسل الجسم بالماء أو بصودا الغسيل النزع النواتج السامة ومعادلة آية زيادة من الحمض